中国医疗器械UDI介绍
本篇文章将从法规、标准、发码机构并以GS1来举例为大家介绍医疗器械UDI的实施。
01/法规
2019年8月,国家药监局发布中国UDI的“基本法”《医疗器械唯一标识系统规则》;
2019年10月,国家药监局公布第一批实施产品目录中涵盖的是III类高风险器械,包括:有源手术器械、无源手术器械、神经和心血管手术器械、医用成像器械、输血、透析和体外循环器械、有源植入器械、无源植入器械、注输、护理和防护器械、眼科器械等共9大类产品,具体产品类别见国家药监局/国家卫生健康委/国家医保局公告(2020年 第106号),实施时间为2021年1月1日。
2021年9月,《关于做好第二批实施医疗器械唯一标识工作的公告》发布,明确在首批实施唯一标识的9大类69个品种基础上,将其余第三类医疗器械(含体外诊断试剂)纳入第二批实施UDI范围,支持和鼓励其他医疗器械品种实施唯一标识。2022年6月1日起,生产的医疗器械应当具有医疗器械唯一标识。
02/标准
YY/T 1681-2019 医疗器械唯一标识系统基础术语
YY/T 1630-2018 医疗器械唯一标识基本要求
YY/T 1752-2020 医疗器械唯一标识数据库基本数据集
YY/T 1753-2020 医疗器械唯一标识数据库填报指南
GB 12904-2008 商品条码 零售商品编码与条码标识
GB/T 16986-2018 商品条码 应用标识符
03/发码机构
(一)中国:
中国物品编码中心(GS1)
中关村工信二维码技术研究院(ZIIOT)
阿里健康科技(中国)有限公司
(二)欧盟:
GS1 AISBL
Health Industry Business Communications Council (HIBCC)
ICCBBA
Informationsstelle für Arzneispezialitäten — IFA GmbH
(三)美国:
GS1
Health Industry Business Communications Council (HIBCC)
ICCBBA
根据以上信息,如果医疗器械厂家满足中国UDI法规要求的同时,需要兼顾到海外监管部门的要求,目前只有GS1一家机构能同时满足中国、欧盟和美国的要求。
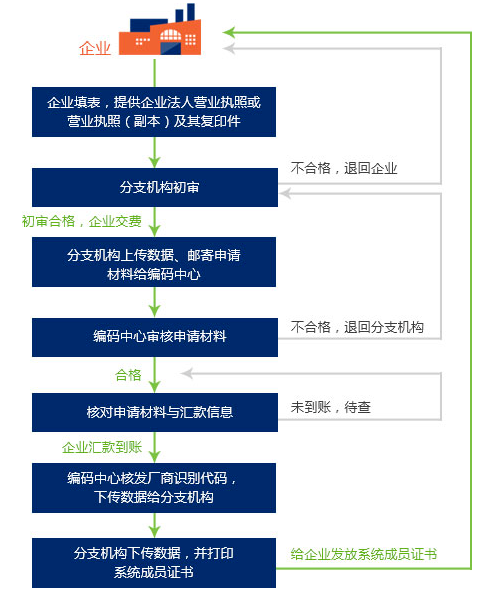
以GS1来举例:申请厂商条码,厂商代码通常有7~10位数字组成,这个代码可追溯到某个特定厂商。厂商代码前三位是前缀码,国际物品编码协会已经分配给中国GS1的前缀码为690~695。我们在申请的时候可以参考GS1的官网,在GS1的官网上面给了比较清楚的步骤:
医疗器械唯一标识包括产品标识和生产标识, 即UDI=产品标识(DI)+生产标识(PI)。UDI的结构示意图如下(摘自YY/T 1630-2018 附录A):
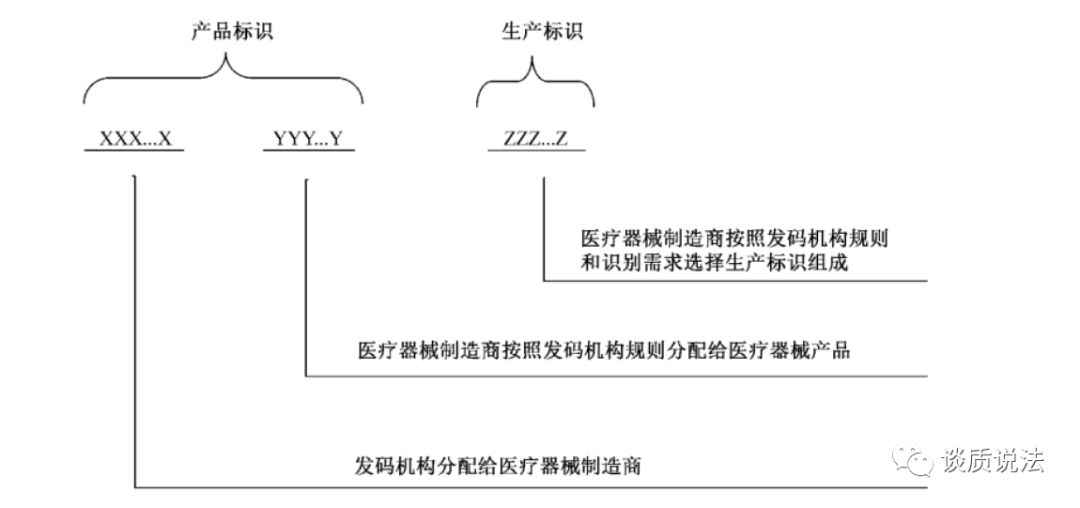
以上图片的产品标识和生产标示只是一个示意图,DI和PI可以是串联,也可以并联的。下面找了两个不同厂家的UDI示例,供大家参考。


UDI规则和GS1的标准的对应关系如下:
|
UDI 法规要求
|
GS1 标准
|
|
UDI-DI
产品标识(DI)
|
GTIN
全球贸易项目编码
Global Trade Item Number
|
|
UDI-PI
生产标识 (PI)
(如适用)
|
AI 应用标识 (AI)
失效日期 AI(17) - e.g. 141120
批次 - 批号 AI(10) - e.g. 1234AB
序列号 AI(21) - e.g. 12345XYZ
生产日期 AI(11) - e.g. 250717
|
|
UDI-DI+UDI-PI=UDI
|
GTIN or GTIN+AI(s) = UDI
|
产品标识UDI-DI:UDI-DI是一个静态信息,用来指明供应链中某个医疗器械的身份信息。在中国,GB 12904中规定了商品条码即GTIN的表示方法。对于医疗器械,最常见的表示方法为GTIN-14,下面我们就以GTIN-14来举例:

上图GTIN-14的第一位(D1)为指示位(indicator),用来指示不同的包装等级;剩下的第2到第13位(D2 - D13)分别包括厂商识别代码、商品项目代码;最后一位(D14)为校验码。厂商识别代码由7-10位数字组成,由中国编码中心负责分配和管理。厂商识别的前3位为前缀码,前缀码由国际物品编码协会分配给中国。商品代码由5-2位数字组成,一般厂商可自行编制。校验码有1位数字,用于检验整个编码的正误。校验码可以自行计算,其方法可以参考标准GB12904-2008的附录B。从实操角度来说,目前很多编码软件能自动计算产生。生产标识 UDI-PI:UDI-PI对应于GS1标准来讲即为应用标识符。它是一个动态信息,其内容通常为序列号、批号、生产日期和有效期(失效日期)等;它属于某个特定医疗器械的动态附加信息,可以跟踪到具体的产品或者批次。根据《GB/T 16986-2018 商品条码 应用标识符 》,应用标识符常见格式如下:

建议医疗器械厂家根据自己的实际情况(以满足追溯的要求)来确定产品的生产标识信息。例如:对于要求追溯到批次的器械,由DI联合PI中的生产日期/有效期、批号实现。对于要求追溯到单品的医疗器械,由DI联合PI中的生产日期/有效期、序列号实现。
来源:网络 原创:苏州市医疗器械行业协会
【声明】部分文章和信息来源于互联网,不代表本订阅号赞同其观点和对其真实性负责。如转载内容涉及版权等问题,请立即与我们联系,我们将迅速采取适当措施。