33企业飞检结果,1家停产整改并全网通报!
11月5日,国家药品监督管理局发布通告要求徐州圣凯斯医疗设备有限公司停产整改。几乎与此同时,辽宁省市场监督管理局也发布了飞检通告,要求32家企业限期整改。以下是具体内容:
采购质控存缺陷,国药监下通牒
近期,国家药品监督管理局组织对徐州圣凯斯医疗设备有限公司进行了飞行检查。检查发现圣凯斯在采购、质控、不良事件监测方面都存在重大缺陷。具体内容如下:
一、采购方面
企业未与控制板、锂电池等主要原材料的供应商签订质量协议,不符合《医疗器械生产质量管理规范》(以下简称《规范》)中企业应当与主要原材料供应商签订质量协议并明确双方所承担的质量责任的要求。
二、质量控制方面
(一)企业注册产品标准规定袖带充气时间、袖带排气时间、袖带耐压强度均为出厂检验项目,以上项目检验时主机逐台连接同一个袖带进行检验,但实际检查发现企业未对不同采购批次的袖带进行相应项目检测,不符合《规范》中企业应当根据强制性标准以及经注册或者备案的产品技术要求制定产品的检验规程并出具相应的检验报告或者证书的要求。

(二)企业产品过程检验(文件编号SKSJL-7.5-02 ,《产品随工,过程检验、老化单》)的调试项目“电池电压”的老化项目只记录了起止时间,未记录老化电压参数,无法判断老化过程中整机是否正常工作;整机充气压力无原始数据,无法判断是否保持在规定范围内;重要元器件控制板的进货检验文件(文件编号SKSJL-7.5-7,《控制板随工、调试、检验单》)“元器件装配、焊接;物资编号标识;按键、指示灯正常、显示内容正常”的检验结果均为“是√”,无原始数据;企业对重要元器件如锂电池、气泵的进货检验只查看外观无破损、文字符号标识是否清晰,查看出厂报告,不符合《规范》中每(批)台产品均应当有检验记录,并满足可追溯的要求。
三、不良事件监测、分析和改进方面
针对有关产品抽检不合格情况,企业未进行有效的不合格原因分析,仅采取了组织检验员再培训的纠正措施,未能提供对同期生产库存产品进行复检的处置记录,未对已销售产品采取召回等处置措施,且检查时企业仍不具备产品输入功率检测能力(如未配备相应检测设备),相关产品仍存在相关项目质控风险,不符合《规范》中对于存在安全隐患的医疗器械,企业应当按照有关法规要求采取召回等措施,并按规定向有关部门报告的要求。
国药监处理措施
该企业生产质量管理体系存在严重缺陷,不符合医疗器械生产质量管理规范相关规定。该企业已对上述其质量管理体系存在缺陷予以确认。
国家药品监督管理局责成江苏省药品监督管理局依法责令该企业停产整改,对涉及违反《医疗器械监督管理条例》及相关法律法规的,依法严肃处理;责成江苏省药品监督管理局责令该企业评估产品安全风险,对有可能导致安全隐患的,按照《医疗器械召回管理办法》的规定召回相关产品。
该企业完成全部项目整改并经江苏省药品监督管理局跟踪复查合格后方可恢复生产。
辽宁省:32家企业限期整改
近日,辽宁省大连市市场监督管理局发布2019年医疗器械经营企业飞行检查情况的通告,4家企业通过检查,32家企业限期整改。以下是此次飞行检查具体情况:
医疗器械经营企业飞行检查情况通告表

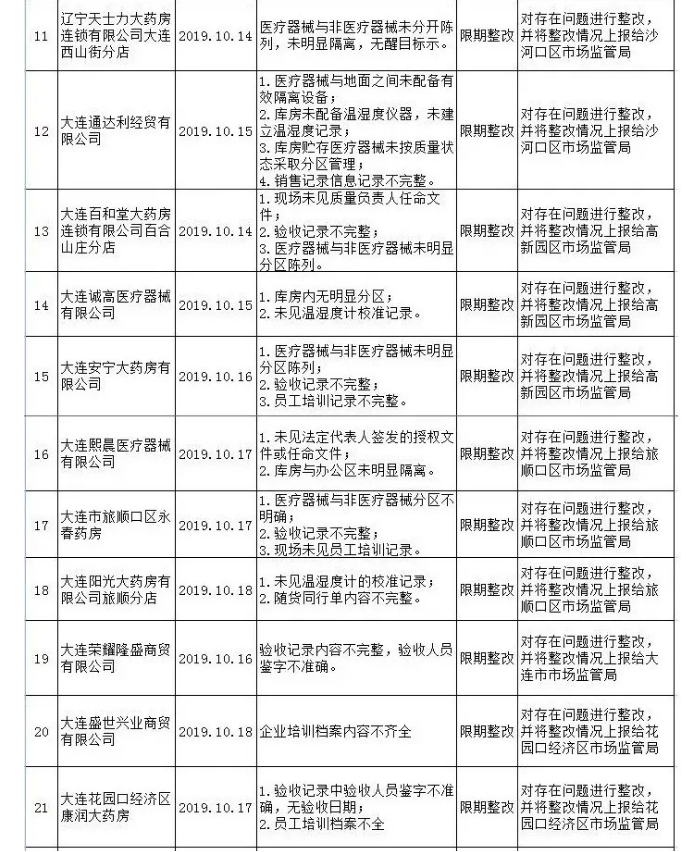

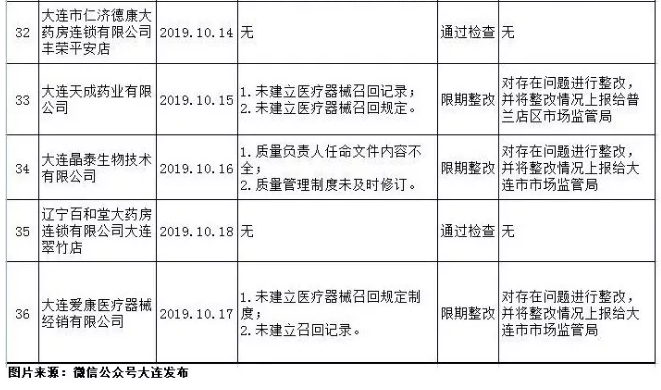
来源:CMDRA
【本文内容为转载,我公司不对本文所包含内容的准确性、可靠性或者完整性提供任何明示或暗示的保证,不对本文观点负责。如转载内容涉及版权等问题,请立即与我们联系,我们将迅速采取适当措施,以保障双方权益,谢谢。】