医疗器械飞行检查情况通告(2023年第3号)

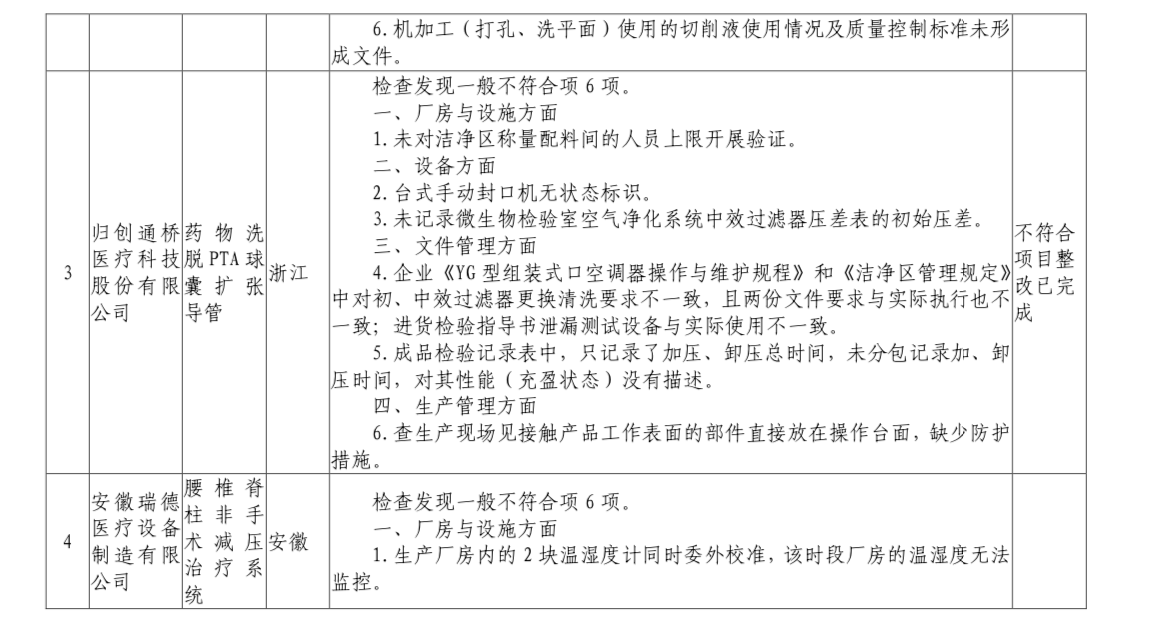
为加强医疗器械监督管理,保障医疗器械安全有效,依据《医疗器械监督管理条例》《医疗器械生产监督管理办法》《药品医疗器械飞行检查办法》《医疗器械生产质量管理规范》及相关附录,以及《食品药品监管总局关于印发医疗器械生产质量管理规范现场检查指导原则等4个指导原则的通知》(食药监械监〔2015〕218号)等要求,按照国家药品监督管理局2023年医疗器械检查工作部署,核查中心于2023年3月组织开展了医疗器械生产企业飞行检查工作,发现北京邦塞科技有限公司等9家企业存在一般项目不符合《医疗器械生产质量管理规范》及相关附录要求;中能医用加速器系统(广东)有限公司存在关键项目不符合《医疗器械生产质量管理规范》及相关附录要求。具体情况见附表。
针对检查中发现的不符合要求问题,请相关省、自治区、直辖市药品监督管理局督促企业按要求整改,要求企业评估产品安全风险,对存在安全风险的,应按照《医疗器械召回管理办法》召回相关产品。企业完成整改后,相关省级药品监督管理局应及时组织对整改情况进行确认,并将确认结果报送国家药品监督管理局食品药品审核查验中心。
附件:核查中心2023年第一批医疗器械飞行检查情况汇总.pdf
国家药监局核查中心
2023年7月3日
附件:














来源:国家药品监督管理局食品药品审核查验中心
【文章内容与信息来源于互联网或转载,我公司不对本文所包含内容的准确性、可靠性或者完整性提供任何明示或暗示的保证,不对本文观点负责。如转载内容涉及版权等问题,请立即与我们联系,我们将迅速采取适当措施,以保障双方权益,谢谢。】
注:文章配图为网络转载图片,侵权即删!