7批次产品召回!涉及史赛克、波士顿科学等知名外企
2月28日,国家药品监督管理局发布了7则召回通告,7批次产品召回均为进口产品,涉及植入式心律转复除颤器、关节假体等。
本次召回的产品共包括4个二级召回,3个三级召回。
值得注意的是,此次波士顿科学召回产品为皮下植入式心律转复除颤器,此前已经出现两起一级召回。其召回原因为:放电治疗过程中出现电压过载的情况,可能会导致严重的不良事件
01
跨国械企频陷“召回门”
据众成数科(JOINCHAIN)统计,2021年,国家药监局、上海市药监局已披露16起波士顿科学产品召回事件,包括6起一级召回,5起二级召回,4起三级召回。一级召回产品为皮下植入式心律转复除颤器、皮下植入式心脏除颤电极导线以及植入式心脏再同步治疗起搏器。
除波士顿科学以外,涉及一级召回还有美敦力、库克医疗、飞利浦、阿姆斯特朗医疗、EUROSILICONE、圣犹达六家跨国医疗器械公司。
其中美敦力2021年共有10起一级召回,涉及产品为胰岛素注射泵、小儿氧合系统、植入式神经刺激电极、植入式再同步治疗心律转复除颤器、覆膜支架系统。其中覆膜支架系统召回原因为:存在在支架移植物部署期间,不透射线标记键有可能会从移植物覆盖组件的远端脱离的问题。
据众成数科(JOINCHAIN)统计,2021年1月1日至2021年12月31日,国家药监局共发布574则产品召回报告,境内召回事件为221起,境外召回事件为353起,占比61%。
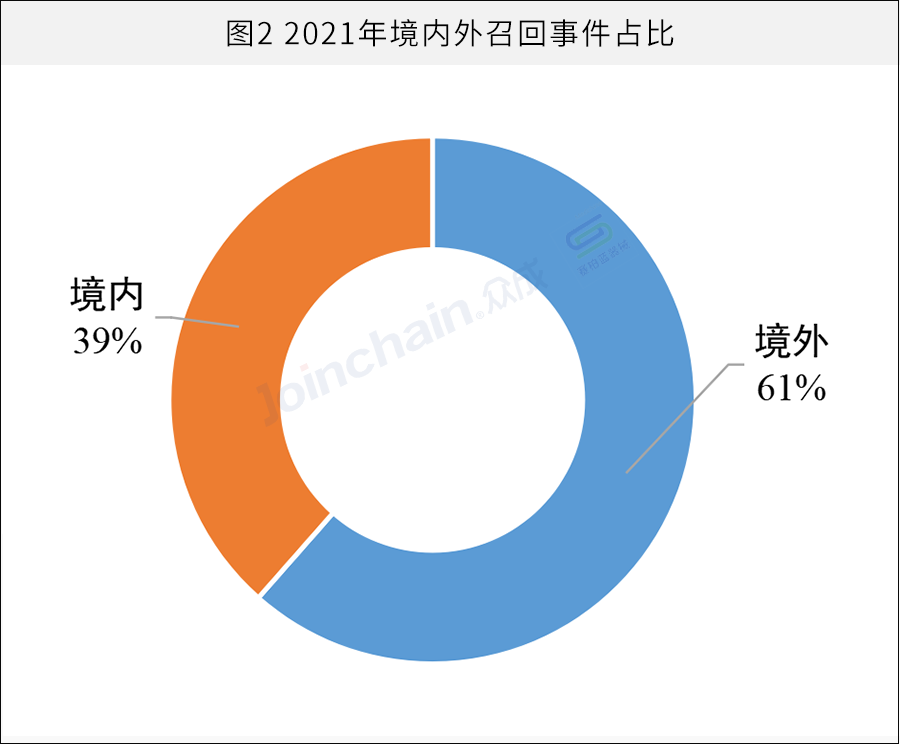
外资企业产品召回多发,与其巨头身份形成鲜明反差,一定程度上反映出企业生产质量把控中的问题,其召回产品多为中高端产品,也侧面体现了在中高端医疗器械外资品牌的掌控力,而境内的产品召回则主要为低值耗材。
02
监管体系不断完善升级
医疗器械医疗器械种类多、跨度大、工艺复杂,如出现产品问题,患者在使用时存在着很大风险。
为了完善医疗器械产品全生命周期质量管理,保障患者的健康,2011年的7月1日,我国《医疗器械召回管理办法(试行)》正式实施,2017年进一步完善,至今已经超10年。
我们需要关注频繁、严重的医疗器械质量问题,督促企业严格把控质量生产关卡,但另一方面也要理解召回本身也是对产品进行不纠错、完善的正常流程。10年来,行业从谈“召回”色变到召回成常态化,也体现来企业对产品召回认知不断提高,主动提升监测手段与风险防控力度。
产品召回制度被认为是产品安全的“最后一道防线”,越来越常态化的产品召回,另一方面也表明了我国医疗器械监管体系逐步完善和严格。
以下为2月28日国家药监局发布的7起产品召回的具体情况:
1、Biomet Trauma对腕部微型锁定接骨板系统DVR Crosslock & ePAK Plating System主动召回
捷迈(上海)医疗国际贸易有限公司报告,由于涉及特定型号、特定批次产品,存在包装袋的无菌封口可能并不都具有足够的密封强度,导致产品无菌包装失效的问题,生产商Biomet Trauma对腕部微型锁定接骨板系统DVR Crosslock & ePAK Plating System(注册证编号:国械注进20153461979)主动召回。
召回级别为三级。
2、Boston Scientific Corporation对皮下植入式心律转复除颤器 Subcutaneous Implantable Defibrillator主动召回
波科国际医疗贸易(上海)有限公司报告,由于涉及特定型号、特定批次产品,存在因低压电容器而导致电池提前耗竭的可能性升高的问题,生产商Boston Scientific Corporation对皮下植入式心律转复除颤器 Subcutaneous Implantable Defibrillator(注册证编号:国械注进20153212410)主动召回。
召回级别为二级。
3、ConvaTec Limited对两件式造口袋 Two-piece ostomy pouch主动召回
康维德(中国)医疗用品有限公司报告,由于涉及特定型号、特定批次产品,存在FUT生产线(CvT,MCH)上生产的造口袋的盖子和袋子本身连接处泄露的问题,生产商ConvaTec Limited对两件式造口袋 Two-piece ostomy pouch(备案凭证编码:国械备20140099)主动召回。
召回级别为三级。
4、Howmedica Osteonics Corp.对髋关节假体EXTER Total Hip System主动召回
史赛克(北京)医疗器械有限公司报告,由于涉及特定型号、特定批次产品,存在标签混淆的问题,生产商Howmedica Osteonics Corp.对髋关节假体EXTER Total Hip System(国械注进20173460477)主动召回。
召回级别为二级。
5、诺贝尔生物公司Nobel Biocare AB对牙科种植体Dental Implant主动召回
诺保科商贸(上海)有限公司报告,由于涉及特定型号、特定批次产品,存在内部六边形不符合规格的问题,生产商诺贝尔生物公司Nobel Biocare AB对牙科种植体Dental Implant(国械注进20153170003)主动召回。
召回级别为二级。
6、强生国际欧洲物流中心Johnson & Johnson International c/o European Logistics Centre对合成可吸收性外科缝线PDS II Polydioxanone Monofilament Synthetic Absorbable Suture主动召回
强生(上海)医疗器材有限公司报告,由于涉及特定型号、特定批次产品,存在部分缝线产品因针线连接处存在裂纹的问题,生产商强生国际欧洲物流中心Johnson & Johnson International c/o European Logistics Centre对合成可吸收性外科缝线PDS II Polydioxanone Monofilament Synthetic Absorbable Suture(注册证编号:国械注进20153023327)主动召回。
召回级别为三级。
7、生物梅里埃法国股份有限公司bioMerieux, SA对巨细胞病毒IgM抗体检测试剂盒(酶联免疫荧光法)VIDAS®CMV IgM (CMVM)主动召回
梅里埃诊断产品(上海)有限公司报告,由于涉及特定型号、特定批次产品,存在校准品RFV值高出可接受范围的问题,生产商生物梅里埃法国股份有限公司bioMerieux, SA对巨细胞病毒IgM抗体检测试剂盒(酶联免疫荧光法)VIDAS® CMV IgM (CMVM)(注册证编号:国械注进20153400764)主动召回。
召回级别为二级。
原创 众成医械 郑文秀
【文章内容与信息来源于互联网或转载,我公司不对本文所包含内容的准确性、可靠性或者完整性提供任何明示或暗示的保证,不对本文观点负责。如转载内容涉及版权等问题,请立即与我们联系,我们将迅速采取适当措施,以保障双方权益,谢谢。】